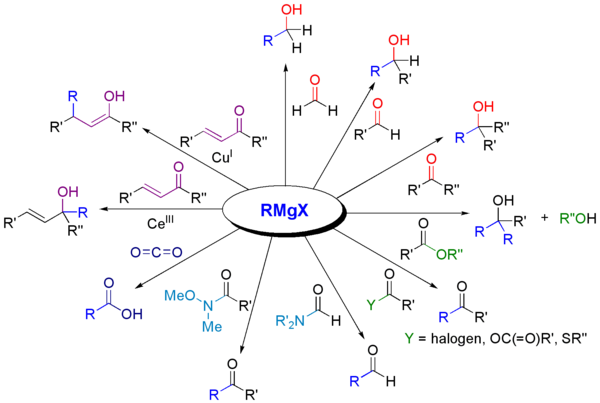
Hvis din carbonylgruppe er koblet til en leaving gruppe, som f.eks. alkoxid'et i en ester eller chlorid'et i en syrechlorid, så får du en nukleofil acylsubstitutionsreaktion, som giver dig en keton. Ketoner er temmelig reaktive, og i tilfældet med esteren vil ketonen være mere reaktiv end startproduktet, og vil være tilbøjelig til at reagere en gang mere. Resultatet er en tertiær alkohol fra en uheldig diaddition.
Hvis du blot benytter en keton, får du i det mindste en monoaddition til carbonylgruppen (1,2-addition), men du får en tertiær alkohol igen. Problemet her er, at du får en uønsket forgrening på det carbon, som du kobler til din phenylring. Du vil have en sekundær alkohol, ikke en tertiær.
En aldehyd giver dig en monoaddition og en sekundær alkohol som produkt, som du kan dehydrere eller eliminere på andenvis, som f.eks. med en tosylering, som du er inde på. Så det er den vej du skal gå. Og igen, jeg tror ikke du skal frygte methoxy-grupperne på phenylringen! De er ret ureaktive, og de skal vist ha nogle tæv før de gider noget!
Mht. metalkatalyse, så er der et væld af overgangsmetaller som giver anledning til smarte krydskoblinger, som ville være umulige at udføre med klassisk syntese. Palladium-katalyse kunne også falde i din interesse.